Vyspělý svět se potýká s nedostupností některých léků. Pacienti v USA, stejně jako v Evropě a stále častěji také v Česku, se marně dožadují léku, na který jsou zvyklí. V poslední době u nás veřejnost zaznamenala, že v lékárnách chybí Framykoin, Torecan či Penicilín. Obvykle je vina svalována na reexporty, ale s tím, jak se mezi evropskými vládami rozšiřuje „infekce“ snižování cen léků a jak si výrobci sami začali hlídat distribuci svých přípravků, jejich význam klesá. Dominují jiné příčiny, zejména pak problémy ve výrobě. Zdravotnický deník zmapoval nejčastější typy výpadků léků na trhu a přináší orientační přehled přípravků, které aktuálně v Česku chybí. Špatnou zprávou je, že se s nedostatkovými léky budeme setkávat i nadále.
Podívejme se nejprve do světa. A zdůrazněme hned v úvodu, že výpadky léků nejsou žádným českým specifikem, nebo projevem neschopnosti našich regulačních či jiných státních úřadů. Jsou fenoménem, s nímž se musíme naučit žít.
Ukázkový případ – BCG vakcína
Před necelým rokem upozornil Wall Street Journal na frustraci lékařů a pacientů z nedostatku některých léků na americkém trhu. Přiblížil ji na příběhu Robin Millerové, 62leté onkoložky z Atlanty, která sama onemocněla rakovinou močového měchýře. Měla dostat potenciálně život zachraňující léčbu, ale lékař jí krátce před jejím zahájením řekl prostě: „Promiň, žádnou nemáme, nemůžeme ti ji dát“. Měl na mysli BCG vakcínu, která najednou nebyla k mání v celých Spojených státech. Objevily se totiž problémy v její výrobě u dvou globálních dodavatelů. Onkoložka Millerová se začala obávat, že se jí bez léku rakovina vrátí a raději si nechala močový měchýř odstranit, udělala tak v nouzi krok, který označila za „barbarský“.
Vakcína BCG (Bacillus Calmette-Guerin) je starý lék, ale stále používaný a nenahraditelný jako očkovací látka proti Mycobacterium tuberculosis, tedy původci tuberkulózy (podává se subkutánně). Osvědčila se však i v onkologii, a to právě specificky u nádorů močového měchýře (aplikuje se přímo do tohoto orgánu).
Mohlo by vás zajímat
V roce 2012 americký úřad FDA (Food and Drug Adminsitration) při rutinní kontrole výroby vakcíny BCG u společnosti Sanofi přímo ve Francii zjistil přítomnost plísně v některých částech aseptických prostor. Výroba byla přerušena a od té doby se vleče výpadek vakcíny na trhu. Další výrobce Merck & Co sice zdvojnásobil výrobu, ale v létě 2014 detekoval znečištění vzduchu ve výrobních prostorách a musel výrobu přerušit. Podle FDA několik málo dalších výrobců ve světě nedokáže v krátkém čase produkci rychle navýšit.
Problémy s BCG vakcínou máme i v Česku u indikace očkování proti tuberkulóze, ale z poněkud jiného důvodu. Nejvýznamnější evropský dodavatel dánská firma SSI zrušila u nás její registraci. Tento krok následoval poté, co Česko ustoupilo od plošné vakcinace, když převážil odborný názor, že její přínos není tak velký (nedostatečná účinnost a přitom vysoká reaktogenita). Paradoxně po zrušení očkování výskyt tuberkulózy poklesl. Nyní se očkují rizikové skupiny novorozenců, v úvahu připadají i migranti a azylanti. Nedostatek dánské vakcíny se nahrazuje polskou vakcínou.
BCG není snadné vyrobit, získává se ze živé bakterie. To ji prodražuje, ale na trhu je 25 let a není již patentově chráněna. V USA stojí jedna lahvička 145 dolarů, což je obrovský rozdíl proti například novějšímu a patentově chráněnému onkologickému léku Avastinu, kde jedna lahvička vyjde na 2700 dolarů. Není divu, že Avastin problémy s výpadky na trhu nemá. Cena BCG je nízká, pojišťovny si ji hlídají. Firmám se jí podařilo za uplynulé dvě desetiletí zvýšit jenom nepatrně a stěžují si, že je demotivuje investovat do zvyšování kapacit nebo kvality výroby. Ještě letos v únoru stále platilo varování před nedostatkem tohoto léku. Tisíce pacientů se ocitlo bez něj, nebo kvůli němu muselo cestovat tisíce kilometrů do zdravotnického zařízení, kde ho ještě mají.
Podle Wall Street Journal ilustruje krize kole BCG vakcíny přetrvávající problém amerického zdravotnictví – nedostatkové léky. Počet přípravků, které nejsou k sehnání, vzrostl v USA za pět let o 74 procent na počet 265, zjistila loni Léková informační služba Univerzity v Utahu. Najdeme mezi nimi velmi širokou paletu různých léků od antibiotik, přes onkologika až po fyziologický roztok. Wall Street Journal se ptal ředitelů firem, nemocničních lékárníků a regulačního orgánu po příčinách výpadků a dozvěděl, že firmy nejsou schopny vybudovat dostatečné výrobní kapacity, nemají dobře udržovaný technický stav svých zařízení a neumí ochránit stárnoucí výrobní linky před kontaminací, čili znečištěním. Přísná opatření ke zvýšení kvality výroby ze strany FDA situaci s dostupností léků ještě dále zhoršují, protože některé firmy reagují uzavřením výrobní linky nebo zmenšováním obejmu výroby během nutných oprav.
Velkou část těchto nedostatkových léků tvoří starší injekční přípravky, které jsou výrobně náročné a nákladné. Současně se ale prodávají za nízké ceny, protože už nejsou pod patentovou ochranou. Firmy nemohou ceny jednoduše zvýšit, neboť proti tomu stojí zdravotní pojišťovny, které si střeží náklady zejména v nemocnicích a u generických léků.
V minulém roce v USA chyběl například také ketorolac, neopioidní lék proti bolesti (příbuzný ibuprofenu), který se hodně používá v nemocnicích na pooperační bolest. Z trhu bylo staženo 18 miliónů balení z důvodu kontaminace částečkami skla. Nedostatkovým se stalo i antibiotikum Zosyn (kombinace účinných látek piperacillin/tazobactam) a jeho generické ekvivalenty, používá se například u zápalu plic. Výrobce originálu gigant Pfizer výpadek zdůvodnil zvýšenou globální poptávkou a neplánovanou odstávkou výrobního zařízení v Itálii. Jiným příkladem je droperidol, psychofarmakum a neuroleptikum (antipsychotikum určeno k léčbě psychóz), u nás používaný v premediakci před anestezií, v USA pak velmi často v ambulancích první pomoci k úlevě od menstruační bolesti hlavy, bolestí břicha a nevolnosti. Začala se zpožďovat výroba a na trhu chyběla také výchozí surovina.
FDA zpřísnil po roce 2009 svoji inspekční činnost, zvláště za hranicemi Spojených států, a to v reakci na skandál s kontaminovanými léky z Číny (o problémech s čínskými substancemi jsme už v ZD psali a také jsme informovali o patálii s bioekvivalenčními zkouškami, které prováděla indická firma). Má tým špičkových zkušených inspektorů, který ze speciálně zaměřuje právě na injekční přípravky. Zároveň ale představitelé FDA dodávají, že firmy jako je Sanofi nemohou mít pocit, že byly “přepadeny” náhle a neočekávatelně, protože na podobné problémy se úřad zaměřuje již vice než 15 let. V roce 2012 byl přijat federální zákon, který posílil pravomoci FDA ve vztahu k nedostatkovým lékům. Úřad tvrdí, že se mu podařilo předejít až 101 výpadkům díky tomu, že nyní více spolupracuje s výrobci při identifikaci možných rizik.
Svět se změnil, trh je zranitelný
Švýcarská firma Birgli AG dala dohromady skupinu expertů z několika zemí, kteří analyzovali příčiny nedostatku léků, se zaměřením na některé státy Evropy a vydali o tom zprávu nazvanou „Birgli Report„. Autoři je rozdělili na předvídatelné a nepředvídatelné a podle frekvence jejich výskytu vytvořili jakýsi žebříček, z nějž je patrné, že převládají v různých podobách problémy ve výrobě (když pomineme přírodní katastrofy, či epidemie).
Příčiny výpadků léků na trhu
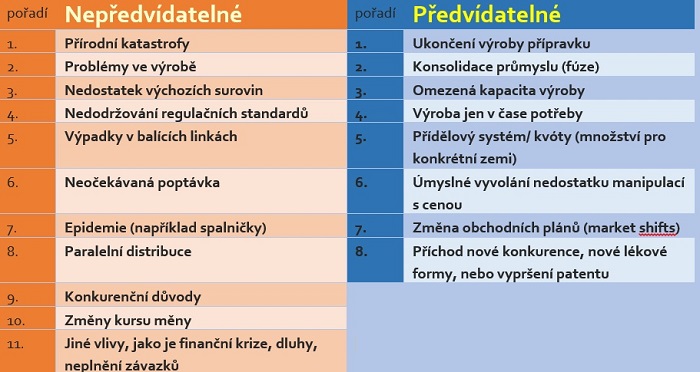
Zpráva poukazuje na úpornou snahu vlád napříč Evropou snižovat ceny léků. Česko bylo jednou z prvních zemí, která začala srovnávat ceny se zahraničím i v rámci skupin vzájemně porovnatelných léků. Proto máme v globále nízké ceny léků, a proto se dařilo i reexportům, tedy skupování léků určených pro český trh a jejich přeprodeji do zemí, kde jsou ceny vyšší, typicky například do Německa (tématu reexportů jsme se věnovali zde). Dnes ale k podobným opatřením přistupují i další státy, čili ceny klesají v téměř celé Evropě a byť stále zůstávají státy, kde se udržuje vyšší cenová hladina, jako je zmíněné Německo, výrobci léků musejí nějakým způsobem reagovat. Cest je několik, ale často volí tu pro pacienty nejméně příjemnou, a to stažení přípravku, jenž přestal přinášet zisk, z trhu (jak vidno z prvního místa v tabulce ve sloupečku předvídatelných příčin). Další reakcí firem je potírání paralelního exportu buď přímými dodávkami do lékáren nebo stanovením kvót, ale ty samy o sobě mohou být příčinou nedostatku léku. Například regulační úřad ve Francii upozornil v roce 2012, že výrobci dodávající své přípravky na základě kvót, neumí pružně reagovat na změnu poptávky.
Výrobní problémy, do kterých se v posledních letech producenti léků dostávají, mají podle „Birgli Report“ kořeny v akvizicích a fúzích. Ty mají za následek koncentraci výroby. Jestliže dříve nějaký lék vyrábělo více farmaceutických firem na více místech a některá z nich měla problémy, pružně jí nahradily ostatní. Nyní je k dispozici méně „továren“ a trh zásobování s léky se stává zranitelnějším. Jakýkoliv incident, který naruší výrobu, téměř vždy komplikuje také distribuci a vede k nedostatku daného přípravku. Omezený počet hráčů na trhu také snižuje konkurenční tlak na kvalitu, v kombinaci se zvýšenou aktivitou lékových regulačních úřadů se pak množí zastavení produkce určitých přípravků z důvodů závady ve výrobním procesu.
Za nedostatkem léků může v některých zemích stát i zpožďování rozhodnutí o jejich hrazení z veřejných rozpočtů. Lékárnám klesá obrat v hrazených lécích, distributoři nemají pohromadě dost peněz, aby platili včas výrobcům a to všechno také vede k přerušení či zpožďování dodávek.
Distributoři v Česku: výpadky přibývají
K výpadkům léků nyní dochází častěji, potvrdili nám i čeští distributoři. Podle Jana Rohbachera, ředitele Alliance Healthcare to lze poznat například na parametru, který se nazývá „servis level“, který udává jak dobře je schopen distributor pokrýt objednávky zákazníků v daném čase. Zatímco dříve dosahoval 80 procent, nyní je na zhruba 70 procentech. „Na náš vrub jdou 3 až 4 procenta, ale zbytek jsou výpadky – chybí náhrada, špatná koordinace dodávek, léky nebyly objednány pro Česko aj. Vždycky nějaké výpadky byly, ale nyní jsou určitě výraznější. Je třeba si ale uvědomit, že máme 460 dodavatelů a 20 tisíc položek,“ vysvětluje ředitel Rohrbacher. Pokud se nedostatek týká dražších léků, používaných zejména v nemocnicích a reexportovaných do ciziny, snaží se je farmaceutické firmy v současnosti ohlídat. Dodávají je přes řízené distribuční kanály a distributoři jako je Alliance jim k tomu zajišťují logistické služby.
„S nedostatkem některých léků se setkáváme poměrně často. Kromě výpadků způsobených reexporty v posledních letech zaznamenáváme i větší počet výpadků způsobený zpřísněnou legislativou – například zpoždění auditu výrobce suroviny, formální opravy příbalových letáků, změny a přeregistrace výrobce, držitele rozhodnutí o registraci či další úpravy. Do výpadku se tak dostávají i banální léky typu Framykoin, za něž se paradoxně náhrada hledá velmi kostrbatě,“ napsal nám Petr Dvořák, ředitel prodeje společnosti Phoenix. Statistiku o tom, jakým dílem se na výpadcích podílejí reexporty, prý ale nejsou distributoři vést. „K dispozici nemáme ani spolehlivé údaje o tom, které objednávky našich zákazníků všech kategorií směřují pro potřeby pacientů a jaké tyto potřeby jsou a kolik jde na reexport,“ dodává Dvořák.
Člen představenstva a finanční ředitel další distribuční firmy Pharmos Radovan Mališ je přesvědčen, že za většinou výpadků stojí samotní výrobci a to kvůli problémům ve výrobě, stahování závadných šarží a logistickým problémům při změně toku distribučních kanálů, což zase souvisí s fúzemi výrobních firem. „Z distribučních kanálů byly vyřazeny klasické velkoobchody, které zajišťovaly standardní dodávky do lékáren, distribuci reexportovaných položek si zajišťují výrobci cestou DTP kanálů (Direct To Pharmacy, přímo do lékáren – poznámka redakce). Takto je dodáváno do lékáren přípravků za více než 9 miliard korun! Nedostatky případně výpadky léčiv jsou často způsobeny také limity určenými výrobci pro jednotlivé lékárny, které neodrážejí aktuální potřeby lékárny,“ míní Mališ. Ředitel z Pharmosu jako příčinu současné situace na trhu s léčivy vidí především v nepřiměřené cenové regulaci. „Důvodem reexportu jsou nízké ceny v porovnání s ostatními zeměmi EU. A právě cenové narovnání trhu je jediná cesta jak předejít exportu léčiv z ČR. Stát připravovanými změnami Zákona o léčivech řeší pouze důsledky tohoto stavu a ne příčiny. Stát by měl zasahovat proti výpadkům léčiv na trhu, už dnes má k tomu ale funkční nástroje, jen je nevyužívá,“ shrnuje R. Mališ.
Podobný názor má i představitel ViaPharmy. „S výpadky léků se setkáváme často – jsou buď trvalé (v případě ukončených dodávek do ČR), anebo dočasné. V druhém případě jde o důsledky reexportů, vadných šarží nebo omezených kapacit výrobce. Podíl reexportů odhadnout neumím. Každopádně jak ty, tak i ukončené dodávky do ČR mají často dva společné jmenovatele – systém referencování cen a podhodnocenou korunu. V poslední době registrujeme výpadky u antibiotických mastí (framykoin, bactroban, ophtalmoframykoin), polyginaxu, isoptinu, carduraxu. Nemyslím si ovšem, že tady jde o důsledek reexportů. Obecně se naši lékárníci shodují, že pokud jde o výpadky, je únor 2016 mnohem lepší než předchozí měsíce,“ uvádí Michal Petrov, tiskový mluvčí nejen ViaPharmy, ale i společnosti Česká lékárna holding (lékárny dr. Max).
Na závady v jakosti jako důvod výpadků léků upozorňuje Linda Prokopová z Asociace evropských distributorů léčiv (AEDL) a dává je do protikladu s reexporty. „Příkladem bylo mimořádné opatření ministerstva zdravotnictví vydané v říjnu 2013 a týkalo se léku NOVOMIX 30 FLEXPEN 100U/ML inj. sus. 5x3ml. Zde je zcela evidentní důkaz, že za výpadkem nestál paralelní distributor, ale sám výrobce,“ říká. Dalším důvodem pro výpadek léků na trhu může podle ní být nespokojenost držitele rozhodnutí o registraci s cenou, za kterou se léčivý přípravek prodává v dané zemi. „Pokud držitel dospěje k rozhodnutí ukončení či přerušení uvádění léčivého přípravku na trh v České republice, dojde k výpadku. Příkladem takového výpadku je léčivý přípravek Antabus (přípravek k léčbě alkoholismu – pozn. redakce). Dalším příkladem vedoucím k dočasným výpadkům při sebemenší odchylce poptávky či nabídky je pomalý, méně účinný a dražší model direct-to-pharmacy. Při výpadku léku, který je v tomto režimu, se pacient musí vrátit k lékaři, požádat o změnu preskripce / terapie, což vede k nárůstu nákladů veřejného zdravotního pojištění,“ kritizuje model DTP Linda Prokopová.
Pokud jde o podíl reexportů na výpadcích léků v Česku, požádali jsme o expertní odhad Jiřího Stránského, ředitele divize Pharma ve společnosti Sprinx Systems, která dlouhodobě český farmaceutický trh monitoruje. „85 % příčin výpadků není zaviněno paralelním exportem,“ zní jeho verdikt.
Pohled regulátora
Aktuálně je v Česku registrováno téměř 56 000 variant léků, z toho je více než 8 000 variant aktivně obchodováno (variantou léčivého přípravku se rozumí léčivý přípravek identifikovaný kódem SÚKL, který je přidělen každému přípravku zvlášť s ohledem na sílu, velikost balení a lékovou formu). V tomto kontextu nevypadají absolutní čísla o nedostatku léků, která ukážeme dále, nijak dramaticky. Týkají se však konkrétních pacientů a v některých případech i nenahraditelných léků.[infobox]
„Vždy záleží na rozhodnutí držitele rozhodnutí o registraci, zda lék bude po úspěšné registraci uveden na český trh nebo ne, případně zda přeruší či ukončí jeho dodávky. Ze zákona však má povinnost o všech změnách v dodávkách (zahájení, přerušení, obnovení, ukončení) SÚKL informovat,“ sdělila ZD mluvčí SÚKL Lucie Šustková. Zákon č. 378/2007, o léčivech stanovuje držiteli rozhodnutí o registraci povinnost oznamovat SÚKL:
– datum skutečného uvedení léčivého přípravku podle velikostí balení a typů obalů na trh v ČR,
a to nejpozději do 2 měsíců po jeho skutečném uvedení na trh,
– datum přerušení nebo ukončení uvádění léčivého přípravku na trh v ČR nejméně 2 měsíce předem; v případě výjimečných okolností lze učinit takové oznámení nejpozději současně s přerušením nebo ukončením uvádění léčivého přípravku na trh v ČR, a to včetně důvodů takového přerušení nebo ukončení,
– datum obnovení uvádění léčivého přípravku na trh, a to neprodleně.
U každého přípravku, u kterého je nahlášeno přerušení či ukončení dodávek, SÚKL vyhodnocuje jeho nahraditelnost. Přípravky, kterými je možné daný lék nahradit, zveřejňuje. „Pokud je SÚKL nahlášeno přerušení či ukončení dodávek u nenahraditelného léčivého přípravku, SÚKL tuto skutečnost neprodleně oznamuje ministerstvu zdravotnictví , které je dle zákona o léčivech oprávněno činit opatření za účelem zajištění dostupnosti léčivých přípravků významných pro poskytování zdravotních služeb,“ vysvětluje mluvčí s tím, že jen od počátku roku 2016 takto SÚKL informoval ministerstvo o celkem 8 léčivých přípravcích.
Informace o změnách v dodávkách na český trh jsou dostupné jednak v databázi léčiv, v detailu přípravku v záložce „Dostupnost“ anebo v Přehledu hlášení o zahájení, přerušení a ukončení uvádění léčivého přípravku na trh. Jak nám také Lucie Šustková prozradila, SÚKL zároveň připravuje další možnost zobrazení (formou excelové tabulky), které by mohlo být jak pro lékaře, tak pro lékárníky více přehledné.
Statistiky hlášení podaných v roce 2015:
zahájení dodávek: 893 kódů SÚKL,
přerušení dodávek: 1.194 kódů,
přerušení dodávek bez následného obnovení: 781 kódů,
obnovení dodávek: 963 kódů,
ukončení dodávek: 773 kódů,
ukončení dodávek bez uvedení nahrazujícího léku: 9.
Jak se postupuje, když v Česku není dostupný konkrétní léčivý přípravek a zároveň je nenahraditelný? V souladu se zákonem existují tyto možnosti:
A) Individuální dovoz (použití neregistrovaného léčivého přípravku) dle § 8 zákona o léčivech
„(3) Při poskytování zdravotních služeb jednotlivým pacientům může ošetřující lékař za účelem poskytnutí optimálních zdravotních služeb předepsat nebo použít i léčivé přípravky neregistrované podle tohoto zákona, pouze za situace, kdy zároveň
a) není distribuován nebo není v oběhu v České republice léčivý přípravek odpovídajícího složení nebo obdobných terapeutických vlastností, který je registrován,
b) jde o léčivý přípravek, který je 1. již registrovaný v jiném státě, nebo 2. přípravkem pro moderní terapie, jehož výrobce je držitelem povolení k výrobě dané lékové formy v rozsahu odpovídajícím povolení k výrobě hodnocených léčivých přípravků vydaným Státním ústavem pro kontrolu léčiv,
c) takový způsob je dostatečně odůvodněn vědeckými poznatky a
d) nejde o léčivý přípravek obsahující geneticky modifikovaný organismus.“
B) Specifický léčebný program
Je jedním ze způsobů zajištění dovozu v ČR neregistrovaného léku pro větší množství lidí. V případě nedostupnosti registrovaného léku, který je určen pro stavy závažně ohrožující lidské zdraví, je možné povolit specifický léčebný program (SLP), který umožňuje distribuci, výdej a použití neregistrovaných léků. SLP schvaluje ministerstvo zdravotnictví na základě stanoviska Státního ústavu pro kontrolu léčiv vždy na určité období. Aktuálně je v ČR povolen SLP u celkem 86 variant léčivých přípravků.
„Výše uvedené alternativy lze použít pouze v případě, kdy je možné léčivý přípravek vyrobit, respektive dodat ze zahraničí, což se však v řadě případů nestává. V posledních několika měsících se množí situace, kdy existuje problém s primárním dodavatelem léčivé látky (potíže ve výrobě, neschopnost doložit kvalitativní parametry účinné látky apod.) a kdy zcela logicky nelze náhradním způsobem zajistit jiný léčivý přípravek. S podobnými obtížemi se tak potýkají i ostatní státy, nejen Česká republika,“ zdůrazňuje mluvčí Šustková a dodává: „V poslední době se ale množí i výpadky související s kvalitou – kdy výrobce, resp. držitel není schopen doložit požadavky na kvalitu přípravku (účinné látky), to je případ Framykoinu.“
Přehled některých léků, které jsou v současnosti nedostatkové (abecedně)
AKTIFERRIN COMPOSITUM cps
- komplex tvořený síranem železnatým a aminokyselinou serin v kapsli, zdroj železa
- ukončení dodávek v 12/215 z důvodu plánovaného ukončení prodeje, na trhu dostupný jen sirup a kapky
- tedy je nahraditelný lékem se stejným složením léčivých látek v jiném množství nebo lékem se stejnými indikacemi s jiným složením léčivých látek
AKTIFERRIN cps
- ukončení dodávek v 12/215 z důvodu plánovaného ukončení prodeje, na trhu dostupný jen sirup a kapky
- je nahraditelný lékem v jiné lékové formě
ASCORUTIN
- rutosid a kyselina askorbová v tabletách – se používají k léčbě zvýšené lámavosti a propustnosti krevních vlásečnic různého původu
- nahlášeno přerušení dodávek k 18. 1. 2016, a to z důvodu neschválení výrobce API (účinné látky)
- nahrazujícím léčivým přípravkem může být lék se stejnými indikacemi
BACTROBAN
- mast na kožní infekce obsahující antibiotikum mupirocin
- od počátku roku bylo již několikrát nahlášeno přerušení a obnovení dodávek (naposledy přerušení k 21. 9. 2015), a to z důvodu výpadku ve výrobě
- nahrazujícím přípravkem je lék se stejnými indikacemi s jiným složením léčivých látek
BACTROBAN NASAL
- mastička do nosu obsahující antibiotikum mupirocin
- přerušení dodávek k 19. 8. 2015, a to z důvodu dočasného výpadku ve výrobě
- přípravek je nenahraditelný, SÚKL o tom informoval MZČR v září tohoto roku
- SÚKL zveřejnil výzvu k předložení návrhu specifického léčebného programu pro přípravek s obsahem účinné látky mupirocinum v září 2015, viz ZDE.
BEROTEC aer. (Berotec N)
- spray obsahující bronchodilatační (průdušky rozšiřující) látku fenoterol určenou k léčbě i předcházení astmatu
- ukončení dodávek z ekonomických důvodů k 31.1.20215, nahraditelný po konzultaci s lékaři
- je možné nahradit jinými léky typu SAMA event. SABA (např. Ventolin N, Ecosal, Berodual N)
DOLGIT tbl.
- lék proti bolesti, obsahující účinnou látku ibuprofen
- přerušení dodávek z důvodu ukončení obchodní spolupráce mezi PRO.MED.CS Praha a.s. a Dolorgiet GmbH.
- přerušení trvá, nahraditelné jiným balením léku
ERYFLUID
- kožní roztok proti akné obsahující antibiotikum erythromycin
- ukončení dodávek v 08/2014 z důvodu plánované (a uskutečněné) žádosti o zrušení registrace, nahraditelné
- lze nahradit přípravkem AKNEMYCIN
FRAMYKOIN, mast
- mast, obsahující kombinaci 2 antibiotik bacitracinu a neomycinu se širokým spektrem účinku, která působí na většinu původců kožních onemocnění způsobených bakteriemi
- výpadek od 08/2015 z důvodu chybějícího výrobce účinné látky, který dosud nemá schválení v registračním řízení, obnovení dodávek melo být 01/2016, ale stále se nerealizovalo
- eventuálně nahraditelný jinými topickými antibiotiky
HALOPERIDOL deconat (Haloperidol Decanoat Richter)
- tablety, obsahující stejnojmennou účinnou látku haloperidol, která patří mezi neuroleptika a působí proti některým těžkým duševním poruchám, poruchám chování a myšlení, zklidňuje a tlumí agresivitu
- nahlášeno přerušení dodávek v období v roce 2012, důvod přerušení není znám
- nenahraditelný
MEGACE susp.
- perorální suspenze s účinnou látkou megestrolem, hormonem, který má zvyšovat chuť k jídlu, a tím i přibývání na váze, používá se k léčení nechutenství a ztráty na váze při zhoubných nádorech nebo při onemocnění AIDS a anorexii
- nahlášeno přerušení dodávek k 3. 8. 2015, a to z výrobních důvodů (dle informací držitele rozhodnutí o registraci bylo plánované obnovení dodávek v září 2015)
- nahrazujícím léčivým přípravkem je přípravek v jiné lékové formě
- SÚKL o nedostupnosti tohoto léčivého přípravku informoval v červenci 2015 MZČR
NITROFURANTOIN-RATIOPHARM
- tobolky obsahující stejnojmenné antibiotikum nitrofurantoin, určené k léčbě infekcí močových cest
- ministerstvo nepovolilo další specifický léčebný program – nahrazujícím přípravkem je FUROLIN. Je ale možný dovoz Nitrofur. z Německa, a to jako individuální dovoz podle zákona o léčivech (lékař předepíše neregistrovaný LP na recept a lékárna objedná ze zahraničí).
OPHTAL
- borová voda s antiseptickým účinkem
- nahlášeno přerušení dodávek k 1. 10. 2015, a to z důvodu zpoždění dodávky
- nahrazujícím léčivým přípravkem je přípravek se stejnými indikacemi
PENDEPON COMPOSITUM INJ PLV SUS
- směs dvou depotních penicilínů v injekci aplikované do svalu (málo rozpustné soli, z nich se penicilin postupně uvolňuje a pacientovi tak stačí jedna dávka na více dnů až týdnů), používá se zejména k prevenci streptokokové infekce například u revmatické horečky, nebo u růže, ale i celé řadě dalších nemocí
- dlouhodobě nedostupný
- k zajištění jeho dostupnosti byl dne 31. 1. 2014 na základě stanoviska ústavu schválen ministerstvem zdravotnictví ČR specifický léčebný program pro přípravek RETARPEN 2.4 M.U.I. Jenže i Retarpen je nedostupný – došlo k přerušení dodávek (není k dispozici surovina) – ten je nenahraditelný.
- na Slovensku dostupný léčivý přípravek PENDEPON COMPOSITUM, který se sice názvem shoduje s léčivým přípravkem v ČR registrovaným, ale léčivá látka obsažená v léčivém přípravku dováženém ze Slovenska je získávána od jiného výrobce a léčivé přípravky nelze považovat za zcela totožné, pokud jde o jejich jakost. S ohledem na skutečnost, že dovážený léčivý přípravek není registrován v ČR, nemůže SÚKL garantovat jeho bezpečnost, jakost a účinnost.
TORECAN IMS+IVN INJ SOL
- injekce proti nevolnosti a zvracení, obsahující thiethylperazin, používá se v onkologii a celé řady různých závažných stavů.
- přerušen od 01/2016 plánované obnovení 04/2016 z důvodu výrobních problémů,
- nenahraditelný
V-PENICILIN SLOVAKOFARMA
- antibiotikum s úzkým spektrem účinku, užívá se např. při lehkých až středně těžkých infekcích – dýchacích cest, uší, zubů, kůže, lymfatických uzlin a cév; spály
- nahlášeno ukončení dodávek k 10. 11. 2014 a k 22. 5. 2015, a to z důvodu změny marketingového záměru a z důvodu nedostupnosti léčivého přípravku v konečné fázi výrobního procesu
- v klinické praxi lze nahradit např. V-PENICILIN MEGA BIOTIKA, PENBENE
Tomáš Cikrt