Zastaralá kritéria pro nasazování biologické léčby, nízká proléčenost pacientů či nesystémová tvorba sítě center – to jsou některé z problémů, které trápí odborníky i pacienty s revmatoidní artritidou. Choroba, kterou v Česku trpí desítky tisíc lidí, přitom může během několika let poslat pacienta do invalidního důchodu, nemluvě o tom, že průměrně zkracuje život o sedm až deset let. Při včasném nasazení optimální léčby lze ovšem u pacientů docílit remise, tedy stavu, kdy mohou žít normální život. Problematice se věnoval seminář, který se konal na konci září v poslanecké sněmovně.
Kdo v minulém století onemocněl revmatoidní artritidou, toho lékaři příliš nepotěšili. K dispozici totiž byla pouze léčba symptomů a příznaků, takže většina pacientů skončila během let v invalidním důchodu. Přelom nastal kolem roku 2000, kdy se objevily první biologické léky. Podařilo se totiž pochopit, jak toto autoimunitní onemocnění vzniká, takže se místo léčby příznaků začalo mluvit o zpomalení destrukce a následně remisi, kdy pacient nemusí užívat léky a nemá žádné problémy.
„Vyléčení to bohužel ještě není, protože se onemocnění může vrátit. Myslím si ale, že do deseti, patnácti let to možné bude,“ říká profesor Karel Pavelka, ředitel Revmatologického ústavu v Praze. V současnosti je přitom snaha dosáhnout u pacientů časné a trvalé remise. Úspěšnost se zvyšuje s tím, když se podaří nasadit adekvátní terapii do 12 týdnů od nastoupení příznaků. Zároveň je dnes trendem tzv. léčba k cíli, která spočívá v tom, že se na začátku stanoví hlavní cíl a pacienti jsou vyšetřováni v tříměsíčních intervalech tak, aby bylo dosaženo remise, případně u pokročilých pacientů nízké aktivity.
Bylo by ovšem mylné domnívat se, že všichni pacienti potřebují biologickou léčbu. Většina z nich dobře reaguje na metotrexát v kombinaci s glukokortikoidy. Pokud dojde k selhání léčby, přichází fáze, kdy pacient buď může, nebo nemusí dostat biologika. K jejich nasazení většinou dojde tehdy, pokud se u pacienta vyskytují prognosticky nepříznivé faktory, je tedy předpoklad, že léčba nebude probíhat příznivě. Jde zejména o mladší pacienty, ženy s vysokou aktivitou choroby a další.
Mohlo by vás zajímat
Switche ano, ale ne administrativní
V Česku je v tuto chvíli registrováno osm biologických léků na revmatoidní artritidu, pět z nich jsou TNF blokátory. Zároveň na trh přicházejí biosimilární přípravky – u infliximabu jsou čtyři a během podzimu by měly přijít na trh také biosimilars adalimumabu. V této souvislosti je přitom na stole otázka takzvaných switchů, tedy záměn léku za biosimilar u rozléčeného pacienta. Podle loňské studie provedené v Dánsku na několika stovkách pacientů s různými diagnózami je záměna možná, zahrnuti ovšem byli jen lidé stabilizovaní. Otazník pak zůstává i nad pacienty s idiopatickými střevními záněty a zelenou nemají ani mnohočetné switche, kdy by si například pacient zašel do lékárny a tam dostal momentálně nejlevnější přípravek.
„Názor odborné společnosti, kde dělám vědeckého sekretáře, je, že switch by měl být sdíleným rozhodnutím lékaře a pacienta. Jsme zatím velmi rezervovaní i k administrativním switchům, tedy nařízením pojišťovny, úředníka, ředitele nemocnice… Také si zatím nemyslíme, že by bylo vhodné, aby to bylo na rozhodnutí lékárníka,“ uvádí profesor Pavelka.
Léčba je podávána v rámci center, jejichž síť je však v Česku značně nerovnoměrná. Vznikala sice na doporučení odborné společnosti, někdy ale pojišťovny nebraly jejich stanovisko v úvahu. Celkem tak dnes funguje 41 center pro dospělé a dvě pro děti, ovšem například na Ostravsku je center kolem desítky, zatímco v celém Plzeňském nebo Libereckém kraji je jen po jednom.
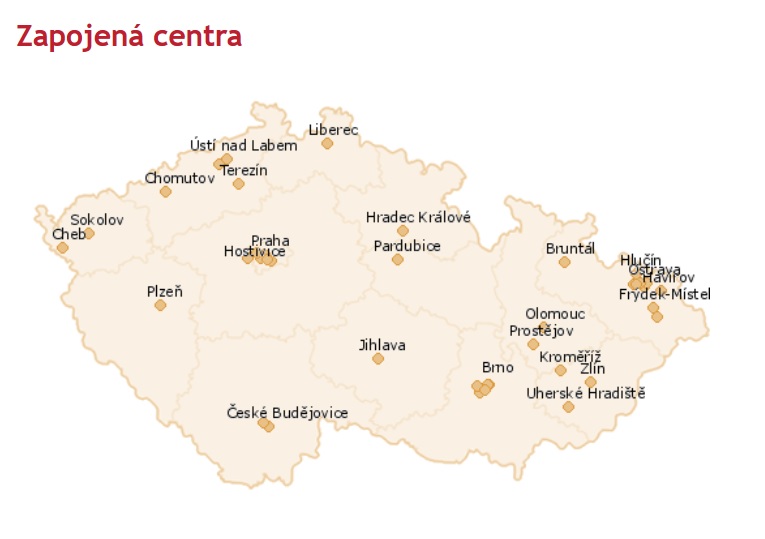
„Bylo zvykem, že když někdo chce nové centrum, napíše na odbornou společnost. My se snažíme být maximálně objektivní v tom smyslu, že hlasujeme, posuzujeme vybavení, dostupnost sestry i lokální potřebu. Jenže jde jen o doporučení a pojišťovny říkají, že to platí, takže rozhodují. V Brně tak máme jedno centrum, které jsme nedoporučili, a na druhou stranu jsou tu dvě další, které jsme doporučili, ale smlouvu dodnes nemají,“ popisuje Karel Pavelka. Některá centra k tomu fungují jen napůl, protože s některými pojišťovnami smlouvu mají, zatímco s dalšími ne. Odborníci by proto stáli o to, aby byla centra vypsána podobně jako komplexní onkologická centra ve věstníku, kde by zároveň byla kritéria, která takové pracoviště musí splnit. Celkem by přitom center mělo být do padesáti, důležitou roli při stanovování sítě by ale měla hrát dojezdová vzdálenost tak, aby to pacienti neměli dále než 40 či 50 kilometrů.
Informace, že pacient dostane levnější variantu léku, může vyvolat nocebo efekt
K tomu, aby bylo možné v praxi sledovat, jaké má drahá biologická léčba efekt, se u nás povedlo zavést jediný registr ve východní Evropě. Celkem se přitom biologickými přípravky léčí necelých 2700 pacientů (více než čtvrtina užívá adalimumab, necelá pětina etanercept, 12 procent tocilizumab, necelá desetina certolizumab a rituximab, devět procent má golimumab, přes osm procent infliximab a šest procent abatacept). K selhání léčby první volby ovšem došlo zhruba u 12 tisíc pacientů a je tedy zjevné, že z biologické terapie by mohlo profitovat více lidí.
Také pokud se podíváme do zahraničí, zjistíme, že proléčenost je tam mnohem větší – zatímco u nás se pohybuje kolem pěti procent, v západních zemích jde o 25 až 30 procent. „Neříkám, že musíme mít tolik pacientů jako v Německu, ale smutné je, že jich mají více už i v Maďarsku a na Slovensku,“ poukazuje Karel Pavelka. Zatímco u nás bylo v roce 2014 léčeno biologickými preparáty 4,2 procenta pacientů, v Maďarsku to bylo devět procent a na Slovensku deset; obdobně jako my na tom bylo Rumunsko.
Stav by snad mohl změnit vstup biosimilárních léků, který by mohl znamenat dostupnost léčby pro více nemocných. „Když se podíváme na onkologii nebo roztroušenou sklerózu, je revmatologie určitou Popelkou,“ konstatuje Edita Müllerová, předsedkyně pacientského sdružení Revma liga.
V souvislosti s biosimilars ovšem poukazuje profesor Pavelka na to, že se u některých pacientů objevuje tzv. nocebo efekt, tedy opak placeba. Když totiž lékař pacientovi řekne, že mu dává levnější variantu léku, aniž by mu problematiku dobře vysvětlil, celá pětina pacientů se do dvou měsíců zhorší. „Tady je pole pro edukaci a spolupráci s pacienty,“ podtrhuje Karel Pavelka důležitost kooperace s pacientskými organizacemi.
Pro zachování produktivity je třeba nasadit léčbu včas
Díky registru také víme, že pacientům bývá při zahájení léčby kolem padesáti let, v té době už ale mají onemocnění zhruba devět let a aktivně jich pracuje jen 40 procent. Pouhá pětina je po selhání jednoho léku, zatímco u zbylých 80 procent selhaly dva, tři nebo čtyři přípravky. Bohužel je také vidět, že zatímco ve vyspělých zemích se výstupy léčby zlepšují, u nás zůstávají obdobné. Podle profesora Pavelky jde o problém v odborných doporučeních, která jsou stará 16 let. I když už ale odborná společnost třikrát napsala nové guidelines, SÚKL je neakceptoval. V poslední verzi z minulého roku už je přitom doporučeno, stejně jako v jiných vyspělých zemích, aby se biologika nasazovala i při střední aktivitě onemocnění. To však prozatím nebylo akceptováno, a tak v tuto chvíli mají lidé vhodní pro biologickou léčbu, ovšem se střední aktivitou choroby, smůlu. „Pacient je nucen čekat, až se mu zhorší zdravotní stav a dosáhne na indikační omezení, která stanovuje SÚKL. Já i celá naše organizace se domníváme, že takový přístup je neetický a zastaralý,“ zdůrazňuje Edita Müllerová.
Tento postup může mít i ekonomické dopady. „Pokud je léčba zahájena až v okamžiku, kdy je pacient jednou nohou v invaliditě, není návrat zpátky navzdory zahájení léčby optimální. Z hlediska podchycení negativního vývoje nemoci je proto potřeba zahájit léčbu včas v okamžiku, kdy pacient začíná mít problémy, klesá mu výkonnost a má krátkodobé pracovní neschopnosti. Pokud se v tu chvíli nezačne léčit, je cesta zpátky z invalidity velice obtížná. Pro ekonomický systém je tak zmařena šance zachovat produktivitu,“ říká Tomáš Doležal z institutu iHETA.
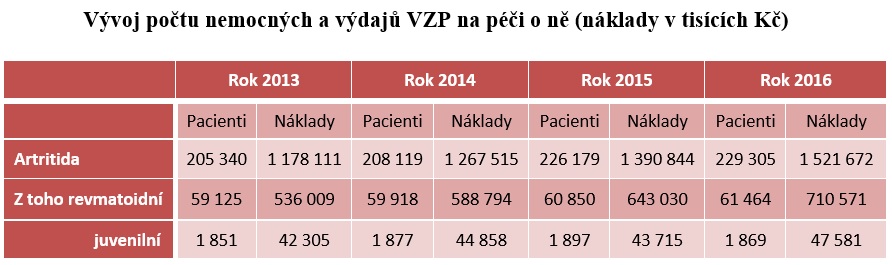
Zachování produktivity přitom vrátí zhruba třetinu nákladů na biologickou léčbu, které se v tuto chvíli podle dat VZP pohybují kolem 220 tisíc za pacienta ročně. Zahraniční data také ukazují, že včasné zahájení terapie pak šetří náklady na chirurgické výkony a hospitalizace v pozdější fázi nemoci, o invalidních důchodech nemluvě. Z našich i zahraničních údajů víme také to, že ne optimálně léčená artritida rychle vede k částečné nebo úplné pracovní neschopnosti. Do deseti let se pak pracovní aktivita propadá pod 50 procent. Podle Doležala přitom jedno QALY (Quality Adjusted Life Year čili získaný rok kvalitního života) vychází podle nejnovějších analýz na 500 tisíc korun, zatímco hranice ochoty platit je 1,2 milionu.
Zatímco rozšiřování indikací se zatím nedaří, pokrok na trhu nečeká. Novinkou je zcela nová kategorie léků, která letos vstupuje na trh, ale nemá ještě úhradu. Jde o takzvané cílené syntetické léky, které vypadají a fungují jako biologické přípravky, ale jde o malé molekuly. A další výhledy do budoucna? Podle profesora Pavelky nastoupí složitější léčebné strategie a také se budou hledat optimální léky pro každého pacienta pomocí genomiky a proteomiky.
Revmatoidní artritida postihuje v Česku kolem 85 tisíc lidí, aktivní onemocnění trápí necelých padesát tisíc. Protože jde o systémovou autoimunitní chorobu, nepostihuje zdaleka jen klouby, ale může zasáhnout i jakýkoliv jiný orgán v těle. Mezi komorbidity patří například kardiovaskulární choroby, přičemž pacienti s artritidou mají téměř dvakrát vyšší riziko infarktu. Dopad má choroba i na délku života, který zkracuje zhruba o sedm až deset let. Pět procent pacientů navíc zemře na posun v krční oblasti. Jediným vnějším vyvolávacím faktorem, který se dosud povedlo prokázat, je kouření.
Michaela Koubová