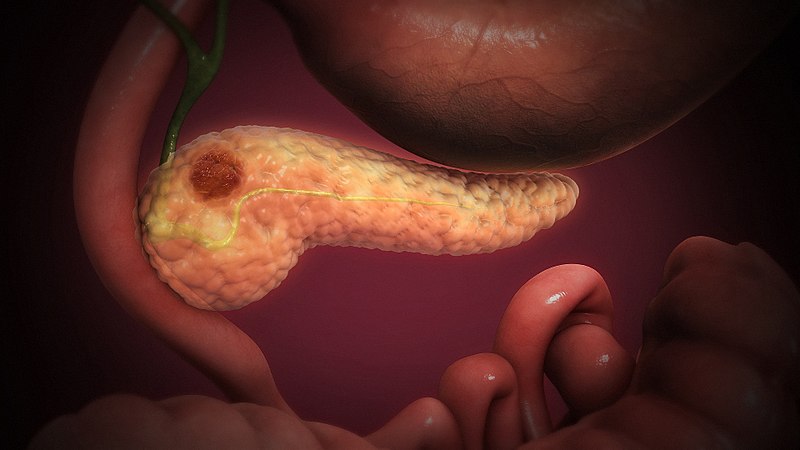
Rakovina slinivky břišní je diagnóza, která má mezi onkologickými onemocněními vůbec nejhorší prognózu. Vědci a lékaři se všemožně snaží pacientům prodloužit život, zatím se ale jako jediná naděje na delší přežití ukazuje včasný chirurgický zákrok v podobě velké resekce. Do budoucna by ovšem mohla být klíčem k úspěchu také molekulární diagnostika, která odhalí mutace, na něž je pak možno cílit léčbu. Zatím je něco takového možné jen zhruba u čtvrtiny pacientů a efekt zdaleka vždy není takový, jaký by si lékaři přáli, jde však o velmi nadějnou perspektivu – ukazuje se, že u necelých deseti procent pacientů je takto možno více než zdvojnásobit přežití oproti veškeré ostatní terapii. Odborníci proto nyní dojednávají s pojišťovnami, aby komplexní molekulární testování u pacientů s rakovinou slinivky hradily.
Prevalence i incidence rakoviny slinivky břišní bohužel v Evropě i Americe stoupá – v ČR je dnes ročně diagnostikována více než dvěma tisícům pacientů ročně. A ačkoliv mezi onkologickými chorobami tvoří dvě procenta, u úmrtí jimi způsobenými už stojí za pěti procenty, takže je čtvrtou nejčastější příčinou smrti na tyto nemoci. Zřejmě se přitom v budoucnu stane druhou nejčastější příčinou úmrtí na rakovinu.
„Podle predikce do roku 2030 lze předpokládat určitý pokles u kolorektálních nádorů, nepatrně u prostaty, ale i u plic, oproti tomu jediný nádor, který do roku 2030 poroste, a to minimálně na trojnásobek oproti dnešní době, je právě slinivka břišní. Tragičnost vyplývá z toho, že pětileté přežití bylo v roce 1987 0,4 procenta a v roce 2005 to bylo skoro stejné číslo – to je ale období, kdy ještě nebyl model onkologické a chirurgické léčby, což jsou jediné cesty, kdy může dojít k prodloužení života. Zlepšení prognózy se děje v kombinaci chirurgie a adjuvantní chemo, případně chemoradioterapie, a to tak, že šance na pětileté přežití se zvyšuje řádově až na desítky procent. Jenže dostatečných resekcí nádoru je dnes i v centrech bohužel jen 40 procent, a to pouze ve skupině 10, maximálně 20 procent pacientů, kteří byli včasně zachyceni a jsou tedy snadno operovatelní,“ vysvětluje přednosta I. chirurgické kliniky – břišní, hrudní a úrazové chirurgie 1. LF UK a VFN Zdeněk Krška. Dnes tak pět let od diagnózy žije osm procent pacientů, u pokročilého onemocnění se ale přežití počítá v měsících.
V Česku je přitom podle Kršky primárně resekabilních sedm až deset procent pacientů; 60 procent už má metastázy. U zbylé skupiny se pak lékaři snaží stanovit biologické chování nádoru a podle toho volí další postup. Faktem však je, že většina pacientů přichází pozdě (a kvůli covidu se situace ještě zhoršila, protože se mnoho pacientů zjara bálo do nemocnice), a biologie nádoru je navíc velmi agresivní a těžko predikovatelná. „Je to onemocnění rezistentní k systémové léčbě, chemoterapii, radioterapii i imunoterapii,“ konstatuje přednosta Onkologické kliniky 1. LF UK a VFN v Praze Luboš Petruželka. Výsledkem je, že jde o karcinom, který má nejhorší prognózu vůbec.
Mohlo by vás zajímat
Přetrvávající problém je nedostatečná koncentrace výkonů
Aby toho nebylo málo, stává se i dnes v Česku to, že se operace tohoto nádoru provádějí na pracovištích, které s nimi nemají dostatečnou zkušenost. Přitom právě velká resekce je v podstatě jedinou nadějí. „Základní roli má chirurg, protože to je jediná šance, která dává nemocným možnost dlouhodobého přežití. Léčba ale není koncentrovaná na chirurgická pracoviště našeho typu,“ poukazuje profesor Petruželka.
„Na některých pracovištích se dělají jednotky operací za rok. Přitom 23 studií prokázalo, že pokud se operace uskuteční ve velkoobjemovém zařízení, je dvakrát vyšší šance na 30denní přežití pacienta. Je tedy strašně důležité, aby pacienti byli operováni na pracovištích, kde operaci provádějí často. Proto by se každý pacient měl ptát, kolik takových operací zařízení ročně dělá. Zároveň bych byl rád, kdyby Česká chirurgická společnost vydala doporučení, jaké je minimum operací, aby pacienti věděli, čeho se mají držet,“ říká výkonný ředitel spolku OnkoMaják Tomáš Kruber, který také poukazuje, že český pacient nyní nemá možnost získat celkový přehled o tom, kolik kde těchto výkonů probíhá.
„Mělo by to dělat pracoviště, které ovládá velké resekce a neudělá jen výkon limitovaný. Přežití se významně zvedá tam, kde se výkon prováděl co nejradikálněji,“ podtrhává Zdeněk Krška. Navíc je nutno náležitě zvážit, zda ještě vůbec operace, která má svá rizika, může pacientovi pomoci a naopak jeho stav nezhorší. Onemocnění tak musí být lokalizované, musí mít nádorové markery, které na léčbu příznivě zareagují, a pacient musí operaci zvládnout (a pochopitelně s ní souhlasit). Pokud se ale i u pokročilého nádoru toto povede splnit a resekce se podaří i s odebráním lymfatických tkání okolo velkých cév, přežívá 40 procent pacientů 40 měsíců.
Zaměření na mutace
K takovému výsledku je ovšem potřeba multioborová spolupráce včetně prediktivního testování. „Ještě v nedávné době jsme běžně slýchali, že karcinom pakreatu je nemoc, kde nemá moc cenu žádné další vyšetřování, protože má špatnou prognózu a nic tam není. To už v současné době neplatí,“ konstatuje přednosta Ústavu patologie VFN a 1. LF UK Pavel Dundr.
Prvním krokem molekulárního a prediktivního testování je diagnostika. Pro další léčbu je přitom zásadní klasifikace a správné zařazení. „Nádorů pankreatu je poměrně hodně, včetně těch tzv. karcinomů slinivky břišní. Většinu představuje duktální adenokarcinom, který má spousty podvariant. Některé z nich jsou agresivnější více, některé o něco méně, ale obecně platí, že jde o nádor agresivní,“ načrtává Pavel Dundr s tím, že mutací u karcinomu pankreatu je široké spektrum – byly popsány u více než 600 genů, z nichž 40 genů má mutace častější než u jednoho procenta pacientů. Jen část z nich je ale bohužel v tuto chvíli nějak terapeuticky ovlivnitelná. „I když ale skoro 80 procent pacientů s karcinomem pankreatu má nějaké aberace, které jsou potenciálně ovlivnitelné, je důležité zdůraznit ono potenciálně. V praxi to tak není,“ dodává Dundr.
Mezi aberace, které se nyní testují a jsou nebo by brzy mohly být ovlivnitelné, patří mutace genů BRCA 1 a 2, které se vyskytují u 7,5 procenta pacientů, dále hodnocení mikrosatelitové instability, která se týká jednoho až dvou procent pacientů, a stanovení mutační nálože, což se týká sedmi procent pacientů. Celkově jde asi o dvacet procent lidí, u nichž by i stávající léčebné možnosti mohly mít větší význam.
„Problém ale může být s interpretací výsledků. Asi není cílem zahltit kliniky žádající o vyšetření seznamem několika set aberací, přičemž nebude jasný jejich klinický dopad. Je tedy třeba vybrat to, co je klinicky významné,“ načrtává Pavel Dundr s tím, že u nás funguje 11 laboratoří, které prediktivní testování provádějí. Například ve VFN pak k interpretaci významu nalezených mutací funguje nádorový board, kde se jednotlivé případy diskutují. Přesto někdy nemusí být odpověď pacienta na léčbu taková, jakou odborníci čekali.
Personalizovaná léčba je zatím hledání jehly v kupce sena
Jaký je tedy dnes postup s největší šancí na úspěch? „Je třeba rychlá diagnostika, staging a okamžitý chirurgický výkon. Kvůli vysokému procentu recidiv je přitom třeba centralizace chirurgické péče, na místě je také zařazení radioterapie do předoperačního schématu léčby. Optimální je pooperační adjuvantní léčba pro všechny nemocné, jinak jim snižujeme šanci. Co se pak týče rezistence na konvenční terapii, je třeba urychleně zavést principy precizní onkologie. Molekulární reflexní testování by mělo být prováděno u všech nemocných, minimum je stanovení BRCA mutace, mikrosatelitové nestability a fúze některých genů. Je třeba urychlit úhrady imunoterapie u mikrosatelitově nestabilních nemocných, stejně jako PARP inhibitorů,“ shrnuje profesor Petruželka.
Co se přitom týče úhrad, vypadá to nadějně. „V září a říjnu jsme s onkology pracovali na tom, abychom s pojišťovnami dostali do praxe komplexní molekulární testování za účelem nejen diagnostickým, ale i prediktivním. Poslední setkání jsme měli před měsícem a ze strany plátců je k tomu velká vstřícnost,“ doplňuje Pavel Dundr.
Do budoucna by se tak měla rozšiřovat precizní medicína umožňující vybrat pro pacienta nejvhodnější léčbu na základě konkrétního genetického znaku. V tuto chvíli je sice podle profesora Petruželky léčba na míru u rakoviny slinivky hledáním jehly v kupce sena, jde ale o perspektivu. Zároveň je podle něj potřeba provádět molekulární diagnostiku u většiny pacientů, abychom byli schopni najít ty, kteří budou mít přínos ze specifické léčby. Proto je také třeba zavádět inovativní léky, byť pro malé počty nemocných.
„Precizní onkologie není pouze virtuální budoucností, což ukazují už současné výsledky. Nemocní, kteří jsou neléčeni v pokročilém stadiu, přežívají mezi dvěma až čtyřmi měsíci. Co se týče současné chemoterapie, u pokročilých onemocnění nemocní přežívají v mediánu méně než jeden rok. Pokud k tomu přidáme léčbu druhé linie, je možno prodloužit jim život o tři až pět měsíců. To je dohromady kolem 14 měsíců. Pokud jde o léčbu na základě biomarkerů, což je zatím pět až deset procent nemocných, tam se můžeme dostat až na 30 měsíců. To je ve smyslu současných výsledků úžasné a měli bychom nemocným tuto léčbu umožnit,“ podtrhává Luboš Petruželka.
Zlepšit situaci by mohl také screening lidí se zvýšeným rizikem. Jde například o pacienty s diabetem III. typu, který vzniká u pacientů s chronickým zánětem slinivky břišní, nebo u lidí s dědičnou zátěží. Plošný screenig, který by odhalil chorobu v bezpříznakovém stadiu, ale zatím nemáme.
Rakovina slinivky se projevuje nespecifickými příznaky, jako je bolest ve střední části zad, žloutnutí očí a pokožky, bezdůvodná ztráta hmotnosti, bolesti břicha, nevolnost či svědění kůže. Bohužel však ve chvíli, kdy začnou být některé z těchto příznaků natolik závažné, že pacienta doženou do nemocnice, bývá na chirurgické řešení pozdě. Primární prevencí je nekouřit, nepřehánět to s pitím a dodržovat zdravý životní styl.
Michaela Koubová