Během tří let, kdy má pražský IKEM k dispozici speciální přístroj umožňující zlepšit stav dárcovského srdce nebo ho převézt na delší vzdálenost, se tímto způsobem povedlo transplantovat 15 pacientů. V době, kdy bojujeme s nedostatkem dárců, se tak rozšiřuje dárcovský pool o orgány, které by jinak nebylo možné využít. O tom, jak program funguje a co je díky němu možné, si ZD povídal s vedoucím programu ex-vivo perfuze srdce v IKEM Miroslavem Koňaříkem.
Kdy a za jakých okolností pořídil IKEM přístroj společnosti TransMedics OCS Heart?
Program ex-vivo perfuze srdce jsme zahájili v říjnu roku 2019. Potřeba implementace této technologie do transplantačního programu IKEM vzešla z existence limitací, které s sebou přináší obor transplantologie. Jde především o nedostatek vhodných dárců a délku tzv. studené ischemie dárcovského srdce. Systém pro ex-vivo perfuzi srdce nám rozšiřuje skupinu vhodných dárců o tzv. ECD dárce, tedy dárce s rozšířenými kritérii (dříve marginální dárce) a o dárce referované z geograficky vzdálených center.
Skupina ECD dárců je charakterizována orgány, které mají přechodně sníženou funkci (mj. v důsledku patofyziologických mechanismů asociovaných se smrtí mozku) – díky modulu pro ex-vivo perfuzi jsme schopni těmto srdcím nabídnout podmínky pro jejich zotavení a po vyhodnocení jejich funkce je použít pro následnou transplantaci. Výsledky takovýchto transplantací jsou ve finále plně srovnatelné s transplantací od standardních dárců. Můžeme tak využít potenciál této doposud opomíjené skupiny dárců.
Můžete přiblížit start projektu?
Mohlo by vás zajímat
Předcházela mu snaha o získání finančních prostředků, neboť systém je z pohledu pořizovací ceny relativně nákladný. Pomoc nabídli sponzoři – Kapka naděje a společnost Shell, kteří systém TransMedics zakoupili. Rád bych jim proto touto cestou ještě jednou poděkoval. Se Všeobecnou zdravotní pojišťovnou bylo jednáno ve věci úhrady jednotlivých perfuzních setů – tedy spotřebního materiálu nezbytného pro každou jednu ex-vivo perfuzi. V neposlední řadě, pro zdárný začátek programu z pohledu personálního obsazení podstoupil tým ve složení profesor Netuka, doktor Ivák, doktor Pokorný a já školení ve výcvikovém centru společnosti TransMedics v USA. To spočívalo v několikadenním kurzu, při němž jsme se technologii na zvířecím modelu učili implementovat do klinické praxe.
Díky přístroji tak nyní máte možnost transplantovat více orgánů…
Vedle toho, že můžeme využít jiný pool dárců, nám systém rovněž umožňuje podstatné zkrácení délky studené ischemie štěpu – tj. druhé zásadní limitace v transplantologii, zvláště významné u transplantací srdce. Jde o interval od okamžiku, kdy přerušíme průtok krve věnčitými cévami do okamžiku jeho znovuobnovení v těle dárce. Srdce je během této doby chráněno podáním tzv. kardioplegického roztoku a uložením do ledové lázně, který zpomalí metabolické pochody v orgánu – nikoliv však zcela zastaví. Délka této kritické periody je přímo úměrná riziku výskytu tzv. selhání dárcovského orgánu. Tato doba by tak ideálně měla být co nejkratší – optimálně do tří, respektive čtyř hodin.
Přístroj vám tedy umožňuje tuto dobu prodloužit?
Ano, a to zásadně. Teoreticky až do intervalu osmi hodin. Díky tomu jsou možné převozy na dlouhou vzdálenost, které by jinak vzhledem k limitu studené ischemie byly nereálné. Takto jsme mohli převézt srdce ze slovenského transplantačního centra v Martině do dětského kardiocentra Motol, kdy celkový čas od odběru dárcovského srdce do jeho transplantace příjemci byl téměř šest hodin. Výsledná studená ischemie štěpu přitom byla zkrácena na 90 minut a výsledek takto provedené transplantace byl a je velmi dobrý.
Kolikrát jste zatím přístroj využili?
V roce 2019 to bylo pouze jednou, v roce 2020 pak rozvoj programu zbrzdil covid, takže jsme provedli jen dvě ex vivo perfuze. O rok později jich bylo pět a letos doposud osm. Počet ex-vivo perfuzí je ale jedna věc, a ta druhá, podstatnější, kolik touto metodou uchovávaných srdcí ve finále můžeme transplantovat. Tato míra využití ex-vio perfundovaných štěpů v našem centru dosahuje 94 procent. V praxi to znamená, že jsme byli schopni úspěšně transplantovat 15 srdcí, které by bez této technologie nemohly být využity.
Využití přístroje tedy roste.
Počet provedených ex-vivo perfuzí dárcovských srdcí v čase stoupá s rostoucí zkušeností dedikovaného týmu a tím, že už je program etablovaný a plně integrovaný do transplantačního managementu Kardiocentra IKEM. Vycházíme přitom z pevně daných indikačních kritérií. V letošním roce jsme díky této metodě provedli osm transplantací srdce – viděno optikou za tento rok dosud provedených transplantací, kterých bylo 39, jde o 20 procent těchto život zachraňujících výkonů nad rámec standardního transplantačního programu.
Jaké dárce tak bylo možno využít?
V 11 případech šlo o dárce s rozšířenými kritérii (ECD dárce). V detailu šlo o šest dárců se stresovou kardiomyopatií, tři s reverzibilní dysfunkcí komor a dva s vysokou dávkou vazopresorické podpory v čase odběru. Předpokladem využití těchto dárců byl příznivý koronarografický nález a důkladné echokardiografické vyšetření. Následná rekondice orgánu spočívající v ex-vivo perfuzi (medián 200 minut) umožnila zotavení funkce a následnou transplantaci srdce.

Takže ve všech případech nešlo jen o zmíněné ECD dárce?
Byly tu i tzv. komplexní indikace – situace, kdy jsou v celém procesu transplantace srdce přítomny dva a více rizikových faktorů jak na straně dárce, tak příjemce. Jedná se např. o čas očekávané studené ischemie nad 120 minut, příjemce po předchozím kardiochirurgickém výkonu, věk dárce nad 55 let či některá z charakteristik ECD dárce. Takové případy byly tři. Pro ilustraci uvádím případ příjemce po již provedené transplantaci srdce a několika předcházejících korekčních výkonech pro vrozenou srdeční vadu. Diskutovaná transplantace tak byla již šestou operací v pořadí. Orgán jsme vezli z Brna, tzn. očekávaná doba studené ischemie štěpu jistě nad 120 min. Ex-vivo perfuzní modul nám tak umožnil uchovávat orgán v optimálním prostředí, podstatně zkrátit dobu studené ischemie a nadto poskytl komfort pro transplantující tým, který měl tak dostatek času pro náročnou preparaci srdce příjemce, která byla komplikována přítomností vazivových srůstů po předchozích operacích. V dalším případě šlo o výše diskutovaný vzdálený odběr s očekávanou délkou studené ischemie nad 240 min.
Můžete přiblížit, jak celý proces odběru a ex vivo perfuze srdce probíhá?
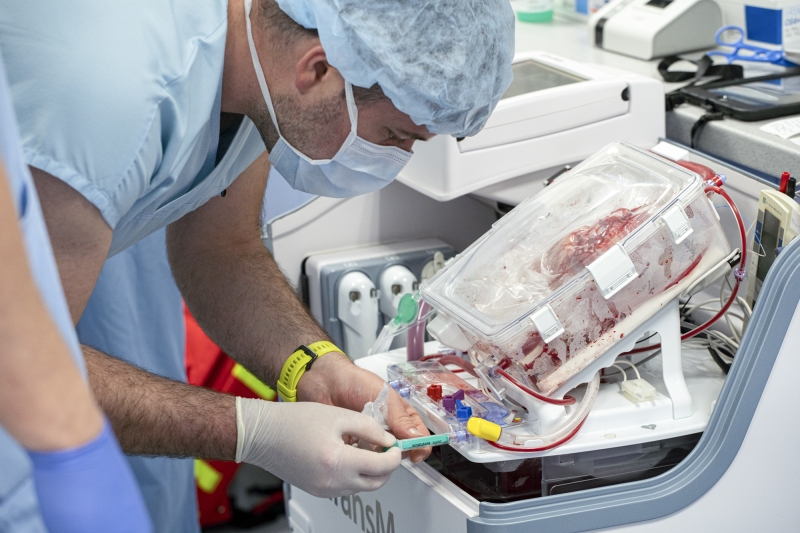
Samotný odběr orgánu se liší především v nutnosti odběru cca 1250 ml krve dárce, která je nezbytnou komponentou perfuzního roztoku v modulu. Následuje naložení svorky na vzestupnou aortu dárce (zastavení průtoku krve věnčitými cévami – začátek tzv. studené ischemie) a podání kardioplegického roztoku, který srdce zastaví v diastole. Orgán vyjmeme z těla dárce, zkontrolujeme případné strukturální abnormity a do vzestupné aorty a plicnice implantujeme k tomu určené kanyly. Paralelně druhá část týmu připravuje perfuzní modul a plní ho perfuzním roztokem, jehož složení optimalizuje tak, abychom orgán umístili do pro něj ideálního prostředí.
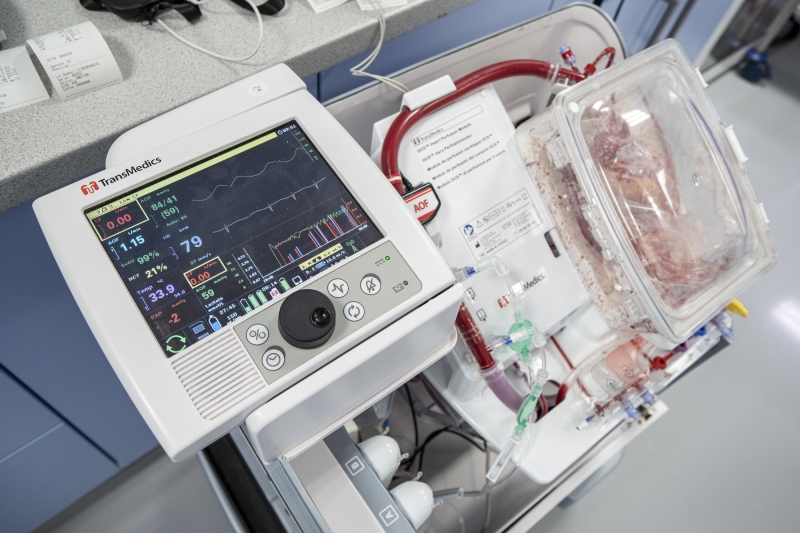
Pomocí výše zmiňovaných kanyl srdce zapojíme do uzavřeného perfuzního okruhu v systému OCS Heart. Perfuzní roztok dominantně protéká řečištěm věnčitých cév (tzv. Langendorffův princip), tzn. nutritivním oběhem srdce. Znovuobnovením krevního průtoku koronárním řečištěm končí interval studené ischemie (tento je tak podstatně zkrácen) a srdce pak buď spontánně či s naší malou pomocí ve formě elektrického výboje opět obnoví svoji aktivitu – začne bít (proces tzv. reanimace). Pro úplnost doplním, že průtok krve zajišťuje pneumatická pumpa, krev je okysličována oxygenátorem a ohřívána tepelným výměníkem. Nespornou výhodou je možnost přepravy tohoto systému jakoukoli formou, včetně leteckého transportu.
A pak přijde fáze, během které se snažíte dostat srdce do lepší kondice…
Ano, v případě srdcí od ECD dárců se snažíme o tzv. rekondici, v případě transportu na velké vzdálenosti pak o zachování již vstupně dobré funkce orgánu. Na rozdíl od konvenčního uchovávání orgánu během ex-vivo perfuze je srdce dárce metabolicky i funkčně aktivní, tedy stahuje se – avšak proti minimálnímu odporu. Srdci tak poskytujeme několikahodinovou úlevu od jakékoliv mechanické práce. Promýváme jej roztokem s adekvátním zastoupením iontů, energetického substrátu a v čase můžeme na potřeby orgánu reagovat jak ve smyslu průtokových charakteristik systému, tak co do korekce složení perfuzátu. K samotnému zotavení přispívá fakt, že orgán v perfuzním boxu není nepřetržitě vystavován negativnímu vlivu neuroendokrinní osy, jako je tomu v těle dárce v důsledku mozkové smrti.
Aktuální kondici orgánu a jeho odpověď na realizované intervence monitorujeme pomocí nepřetržitě měřených hemodynamických parametrů a hodnocením metabolického stavu orgánu, nepřímo tak jeho funkce. Sledovaným biomarkerem je hladina kyseliny mléčné (laktátu) v perfuzním roztoku, respektive změna její koncentrace v čase. Známkou správně vedené ex-vivo perfuze je konstantní či klesající hladina laktátu v čase. Takovýto orgán je následně vyhodnocen jako vhodný k transplantaci. V opačném případě, tedy při negativním trendu laktátu či při nemožnosti dosáhnout cílových perfuzních parametrů, máme evidenci o neúspěšné rekondici a takovýto orgán není využit pro transplantaci příjemci (v našem souboru doposud jeden případ).
Bude u nás díky přístroji ještě možné dále pool dárců rozšířit?
V zahraniční již probíhá program transplantace srdce od dárců po nezvratné zástavě oběhu (tzv. DCD dárci), což je další skupina v ČR dosud nevyužívaných dárců, která má bezesporu potenciál navýšit počty provedených transplantací srdce. Srdce je v tomto případě zapotřebí resuscitovat po epizodě tzv. teplé ischemie a poskytnout mu čas k zotavení v optimalizovaném prostředí, které poskytuje právě box pro ex-vivo perfuzi. Započali jsme spolupráci s vybranými dárcovskými centry, které mají s problematikou DCD dárců zkušenosti. Naší ambicí je zahájit program DCD transplantací srdce počátkem roku 2023.
Jak funguje hrazení programu, je s pojišťovnami nastaveno optimálně, nebo je co vylepšovat?
Určitě si nemůžeme stěžovat. Máme nasmlouvaný určitý počet perfuzních setů pro daný rok – prozatím se zdá, že tento počet plně pokrývá reálné potřeby našeho pracoviště. Díky této technologii roste počet ročně provedených transplantací srdce. Klesá tak naopak počet nemocných, kteří by vyžadovali implantaci dlouhodobé mechanické srdeční podpory jako tzv. „mostu k transplantaci srdce“, takže ve finále zdravotní pojišťovna ušetří v nákladech za tento mezikrok v léčbě pacientů s refrakterním srdečním selháním.
Foto: IKEM
Michaela Koubová